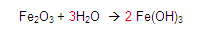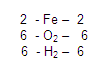Una función química es un conjunto de
compuestos que tienen propiedades muy parecidas en virtud a que sus moléculas
contienen uno o más átomos iguales (grupos funcional).
Se considera como grupo funcional
a un átomo o grupo de átomos que son los responsables del carácter químico de
la molécula a la que pertenecen.
Principales
funciones químicas inorgánicas
·
Óxidos básicos
·
Óxidos ácidos
·
Hidruros
·
Hidróxidos
·
Oxiácidos
·
Hidrácidos
·
Oxisales
·
Sales haloideas
La fórmula química es la representación convencional de los elementos
que forman un compuesto o molécula. En la fórmula química se indican los
elementos presentes en la molécula, y con un subíndice el número de átomos de
cada elemento.
Se llama valencia química a la
capacidad de combinación de un elemento químico determinado con respecto a
otros elementos, cuando forman entre sí diferentes compuestos.
El número de oxidación se
define como la carga eléctrica que tiene un átomo en un compuesto químico.
Principales
nomenclaturas que se usan para nombrar los compuestos químicos inorgánicos:
Hay tres tipos de nomenclatura: La Tradicional, la Stock (la más utilizada) y
la Sistemática o IUPAC (Unión Internacional de Química Pura y Aplicada).
Nomenclatura sistemática
Se utilizan prefijos numerales numéricos (mono, di, tri, tetra, penta, hexa,
hepta)
que indican la cantidad de átomos.
Ejemplos:
Monóxido de carbono, pentóxido de diarsenico,
bióxido de plomo, dihidróxido de mercurio.
Nomenclatura de Stock
Se utilizan números romanos entre paréntesis, para indicar el número de oxidación del elemento, a
continuación del nombre de dicho elemento. Si el número de oxidación es invariable
no es necesario indicarlo.
Ejemplos:
Cloruro de hierro (III), óxido de cobre (I), sulfato de oro (III), hidróxido de
plomo (IV).
Nomenclatura tradicional
Es el sistema más antiguo y consiste en designar el estado de mayor número de
oxidación con la terminación ico y
el de menor número de oxidación mediante la terminación oso. Cuando el número de oxidación es invariable puede emplearse
solo el nombre del elemento. Cuando el elemento presenta más de dos estados de
oxidación se emplean además los prefijos hipo
y per, como se señala a continuación.
Valencia Nombre
1 – 2 Hipo __ oso
3 – 4 __ __ oso
5 - 6 __ __ ico
7 Per __ ico
Ejemplo:
Anhídrido hipocloroso, anhídrido cloroso, anhídrido
clórico, anhídrido perclórico
:) Es hora de practicar .... ejercicios a solo un clic